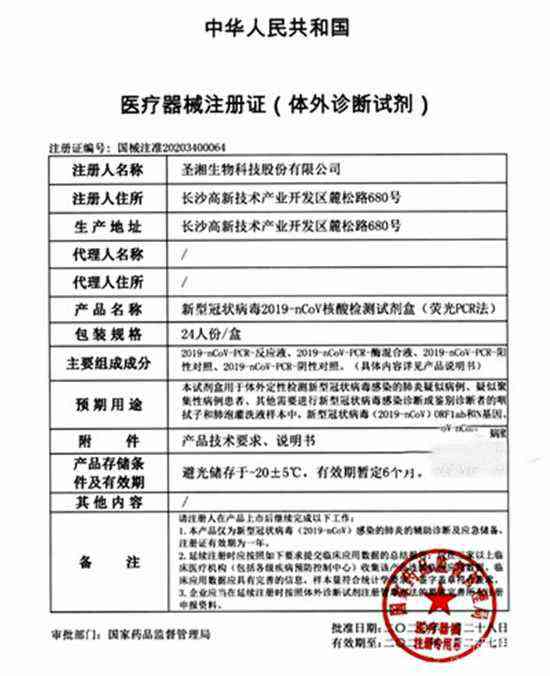
中国新报讯(通讯员 李送君)昨晚,圣湘生物透露,圣湘生物新型冠状病毒2019-nCoV核酸检测试剂盒(荧光PCR法)通过国家药品监督管理局审批,获得医疗器械注册证书。这意味着该产品通过国家药监部门严格的质量体系考核,其安全性、有效性及质量可控性等获得国家药监部门认定,将全面助力疫情防控。

新型冠状病毒感染的肺炎疫情刚开始在武汉发生时,圣湘生物便成立了以国家特聘专家、中国体外诊断领军人物戴立忠领衔的疫情防控应急技术攻关小组,联合军事科学院军事医学研究院,并基于公司10余年的技术沉淀和数亿人份产品应用积累经验,于1月14日成功研制出新型冠状病毒核酸检测试剂盒。
该项目研究得到了科技部应急专项支持,产品采用圣湘生物独创的“RNA一步法”技术,可适用于不同应用场景,操作简单,检测耗时短,灵敏度为200copies/mL,全程内源性管家基因监控,样本处理与扩增检测在一个PCR反应管中即可完成,最大程度减少生物安全风险和交叉污染。该产品通过简单的样本处理后可直接在常规荧光PCR仪上使用,1个操作人员在2小时内(前处理仅需10分钟)可以完成96份样本的检测;结合圣湘生物自主研发的全自动核酸提取仪,单批检测样本量可达96人份,能实现1人1机1日检测样本量达1000人份以上的高通量检测;结合圣湘生物移动分子诊断平台(POCT),最快可在30分钟出检测结果,实现现场即时检测。
在1月26日上海市新型冠状病毒感染的肺炎疫情防控工作新闻发布会上,上海市预防医学会会长吴凡表示,此次新型冠状病毒感染肺炎出现了轻症感染者和“隐形病人”。这些患者本身或症状较轻不易引起重视、或没有症状,但处在潜伏期和隐性感染期,均可能传播病毒。
在1月28日国家卫生健康委召开的新闻发布会上,国家医疗专家组成员、北京地坛医院感染性疾病诊疗与研究中心首席专家李兴旺也表示,在散发病例密切接触者中,观察到一些无症状的感染者,虽然没有症状,但是做核酸检测是阳性的。
疑似病例特别是隐性感染者得到精准快速的诊断,通过快速筛查分流,切断传播源,防范交叉感染,是控制疫情的关键。但大部分医疗机构每天能够检测的数量只有数百人份,检测耗时长,导致疑似病例筛查、分流和确诊周期长,进一步增加交叉感染机会。
圣湘生物董事长戴立忠表示,该公司新型冠状病毒2019-nCoV核酸检测试剂就是根据当前疫情控制痛点难点进行设计的,能够为疫情防控提供快速、简便、精准、高通量的核酸检测方案,有效助力识别疑似病例特别是隐性感染者,快速分流患者,防止交叉感染,避免更大范围的疫情扩散。
面对突发疫情应急物资短缺的需求,圣湘生物春节假期紧急调配员工返岗,组织研发生产,所有生产线满负荷工作,新型冠状病毒核酸检测试剂日均产能最高可达50万人份。
相关热词搜索:









